Osmose (, também nos EUA) denota a translocação líquida inerente de moléculas de solvente através de uma membrana seletivamente permeável, procedendo de uma região de potencial hídrico elevado (caracterizada por uma concentração mais baixa de soluto) para uma área de potencial hídrico reduzido (possuindo uma concentração mais alta de soluto). Esse movimento visa equilibrar as concentrações de soluto em ambos os lados da membrana. Alternativamente, pode caracterizar um processo físico onde qualquer solvente atravessa uma membrana seletivamente permeável (que é permeável ao solvente, mas não ao soluto), separando duas soluções de concentrações diferentes. A osmose é capaz de realizar trabalho. A pressão osmótica é delineada como a força externa necessária para impedir o movimento líquido do solvente através da membrana. Esta pressão é uma propriedade coligativa, significando a sua dependência da concentração molar do soluto e não da sua identidade específica. O transporte osmótico é facilitado pelo fluxo viscoso do solvente sob um gradiente de pressão.
Osmose (, EUA também ) é o movimento líquido espontâneo de moléculas de solvente através de uma membrana seletivamente permeável de uma região de alto potencial hídrico (região de menor concentração de soluto) para uma região de baixo potencial hídrico (região de maior concentração de soluto), na direção que tende a equalizar as concentrações de soluto nos dois lados. Também pode ser usado para descrever um processo físico no qual qualquer solvente se move através de uma membrana seletivamente permeável (permeável ao solvente, mas não ao soluto) separando duas soluções de concentrações diferentes. A osmose pode ser feita para funcionar. A pressão osmótica é definida como a pressão externa necessária para evitar o movimento líquido do solvente através da membrana. A pressão osmótica é uma propriedade coligativa, o que significa que a pressão osmótica depende da concentração molar do soluto, mas não da sua identidade. O transporte osmótico ocorre através do fluxo viscoso do solvente sob um gradiente de pressão.
A osmose representa um mecanismo crucial nos sistemas biológicos, principalmente porque as membranas biológicas exibem semipermeabilidade. Geralmente, essas membranas são impenetráveis por estruturas moleculares substanciais e polares, como íons, proteínas e polissacarídeos. Por outro lado, eles são permissivos a compostos não polares ou hidrofóbicos como lipídios, juntamente com pequenas moléculas, incluindo oxigênio, dióxido de carbono, nitrogênio e óxido nítrico. A permeabilidade depende da solubilidade, carga elétrica, propriedades químicas e dimensões do soluto. As moléculas de água atravessam a membrana plasmática, a membrana tonoplástica (vacúolo) ou as membranas das organelas através da bicamada fosfolipídica por meio de aquaporinas, utilizando um mecanismo seletivo de fluxo de poros. A osmose constitui o principal método pelo qual a água é transportada para dentro e para fora das células. A pressão de turgescência dentro de uma célula é sustentada principalmente por processos osmóticos que ocorrem através da membrana celular, entre o interior celular e seu ambiente comparativamente hipotônico.
Histórico
Evidências de fenômenos osmóticos têm sido observadas desde a antiguidade, por exemplo, em contextos relacionados à construção das pirâmides egípcias. Jean-Antoine Nollet forneceu a observação documentada inicial da osmose em 1748. O termo "osmose" origina-se das palavras "endosmose" e "exosmose", que foram formuladas pelo médico francês René Joachim Henri Dutrochet (1776-1847) a partir das palavras gregas ἔνδον (éndon "dentro"), ἔξω (éxō "externo, externo"), e ὠσμός (ōsmós "empurrar, impulsão"). Em 1867, Moritz Traube desenvolveu membranas de precipitação altamente seletivas, melhorando assim a metodologia e a precisão da medição do fluxo osmótico.
Descrição
Osmose refere-se à translocação de um solvente através de uma membrana semipermeável na direção de uma maior concentração de soluto. Em contextos biológicos, o solvente é caracteristicamente água, mas a osmose também é observável em líquidos alternativos, líquidos supercríticos e até gases.
Quando uma célula é imersa em um meio aquoso, as moléculas de água atravessam a membrana celular de uma região caracterizada por uma concentração mais baixa de soluto para outra com uma concentração mais alta de soluto. Ilustrativamente, quando uma célula é imersa numa solução salina, as moléculas de água saem do interior celular. Por outro lado, se uma célula for imersa em água doce, as moléculas de água entrarão na célula.
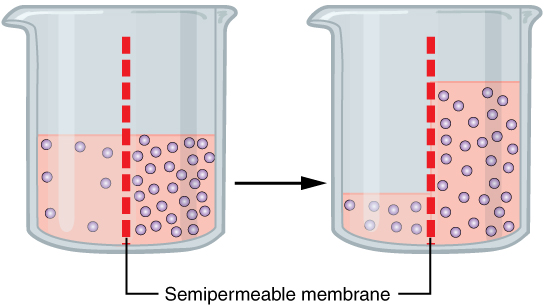
Quando a membrana separa volumes idênticos de água pura em lados opostos, as moléculas de água translocam-se bidirecionalmente a uma taxa equivalente. Consequentemente, há uma ausência de translocação líquida de água através da membrana.
A osmose é observável quando fatias de batata são introduzidas em uma solução com elevada concentração de sal. A água do interior da batata migra para a solução circundante, resultando no encolhimento celular e na redução da pressão de turgescência. Existe uma correlação direta entre a concentração da solução salina e a magnitude da redução nas dimensões e massa da fatia de batata.
Os jardins químicos ilustram o fenômeno osmótico no domínio da química inorgânica.
Mecanismo
O mecanismo subjacente que conduz a osmose é suscetível de interpretação errônea como a diluição da água pelo soluto (levando a uma concentração diminuída de água no lado de maior concentração de soluto da membrana e, consequentemente, estimulando a difusão da água ao longo de um gradiente de concentração) ou, alternativamente, como resultado da afinidade de um soluto pela água (reduzindo assim a disponibilidade de água livre no lado de maior concentração de soluto da membrana e induzindo assim uma translocação líquida de água em direção ao soluto). No entanto, ambas as conceituações foram definitivamente refutadas.
O modelo de difusão da osmose é considerado insustentável porque a osmose pode facilitar o movimento da água através de uma membrana em direção a uma região de maior concentração de água. Da mesma forma, o modelo de "água ligada" é refutado pela observação de que a osmose opera independentemente do tamanho da molécula de soluto - uma característica das propriedades coligativas - e de sua hidrofilicidade.
A descrição precisa da osmose requer uma estrutura mecânica ou termodinâmica, pois envolve fundamentalmente uma interação entre o soluto e a água que neutraliza a pressão que as moléculas de soluto livres exerceriam de outra forma. Notavelmente, o calor ambiente pode ser convertido em energia mecânica, como a subida da água. Consequentemente, o transporte osmótico de solvente é caracterizado como um fenômeno impulsionado pela pressão, em vez de um processo de difusão molecular aleatória. Numerosas explicações termodinâmicas investigam o conceito de potencial químico, elucidando como o comportamento da água dentro de uma solução se desvia daquele da água pura. Esta divergência surge do aumento da pressão e da presença de solutos, que coletivamente neutralizam as mudanças, mantendo assim um potencial químico constante. O teorema virial ilustra que a atração intermolecular entre as moléculas de água e de soluto diminui a pressão geral. Conseqüentemente, a pressão exercida pelas moléculas de água umas sobre as outras em uma solução é menor do que na água pura, permitindo que a água pura conduza o movimento para dentro da solução até que o equilíbrio da pressão seja alcançado.
Significado Biológico
A pressão osmótica serve como mecanismo primário de suporte estrutural em numerosas espécies de plantas. O influxo de água impulsionado osmoticamente eleva a pressão de turgescência exercida contra a parede celular até que ela se equilibre com a pressão osmótica, estabelecendo assim um estado estacionário.
Quando uma célula vegetal é imersa em uma solução hipertônica em seu citoplasma, a água sai da célula, fazendo com que ela encolha. Este processo torna a célula flácida. Em casos graves, a célula sofre plasmólise, onde a membrana celular se desprende da parede celular devido à pressão interna insuficiente da água.
Por outro lado, quando uma célula vegetal está situada em uma solução hipotônica ao seu citoplasma, a água entra na célula, levando à sua expansão e resultando em um estado túrgido.
A osmose também é extremamente importante nas células humanas, onde medeia o transporte de água através das membranas celulares. Este mecanismo é indispensável para preservar a hidratação celular adequada, dada a sensibilidade das células tanto à desidratação como à hiperidratação. Nas células humanas, a osmose é fundamental para regular o equilíbrio da água e dos solutos, garantindo assim um desempenho celular ideal. As interrupções na pressão osmótica podem precipitar a disfunção celular, ressaltando o papel vital da osmose na manutenção da saúde e da integridade estrutural das células humanas.
Sob condições ambientais específicas, a osmose pode ser prejudicial aos organismos. Por exemplo, peixes de aquário de água doce e salgada morrem rapidamente se forem introduzidos em água com salinidade inadequada. O efeito osmótico letal do sal de cozinha em sanguessugas e lesmas fornece outra ilustração de como a osmose pode causar danos às entidades vivas.
Considere o cenário em que uma célula animal ou vegetal é imersa em uma solução aquosa contendo açúcar ou sal.
- Se o meio circundante for hipotônico comparado ao citoplasma da célula, a célula absorverá água por osmose.
- Se o meio for isotônico, nenhum movimento líquido de água ocorrerá através da membrana celular.
- Por outro lado, se o meio for hipertônico em relação ao citoplasma da célula, a célula sofrerá perda de água por osmose.
Consequentemente, uma célula colocada em uma solução com uma concentração de soluto mais alta do que seu ambiente interno sofrerá crenação (enrugamento), enquanto uma célula situada em uma solução com uma concentração de soluto mais baixa irá inchar e potencialmente sofrer lise (estourar).
Fatores que influenciam
Pressão Osmótica
A osmose pode ser neutralizada elevando a pressão na região de maior concentração de soluto em relação à região de menor concentração de soluto. A força por unidade de área, ou pressão, necessária para inibir a passagem de água (ou qualquer outra solução altamente fluida) através de uma membrana seletivamente permeável para uma solução mais concentrada define a pressão osmótica dessa solução, também conhecida como turgor. A pressão osmótica é classificada como uma propriedade coligativa, indicando sua dependência apenas da concentração do soluto, e não de sua composição química ou identidade específica.
Gradiente Osmótico
Um gradiente osmótico representa o diferencial de concentração entre duas soluções separadas por uma membrana semipermeável, servindo para quantificar a disparidade percentual de um soluto específico dissolvido.
O gradiente osmótico é tipicamente observado em sistemas compreendendo soluções separadas por uma membrana semipermeável, o que facilita a difusão da água em direção à solução hipertônica, caracterizada por uma maior concentração de soluto. Eventualmente, a pressão hidrostática exercida pela coluna de água no lado hipertônico se equilibra com a pressão osmótica do lado hipotônico, que possui menor concentração de soluto, estabelecendo assim o equilíbrio. Ao atingir o equilíbrio, o movimento da água persiste, mas ocorre bidirecionalmente com igual magnitude e força, estabilizando assim a solução.
Variações
Osmose Reversa
A osmose reversa constitui um processo de separação que emprega pressão para conduzir um solvente através de uma membrana semipermeável, que retém solutos de um lado enquanto permite a passagem do solvente purificado para o outro. Este processo força o solvente de uma região de alta concentração de soluto através da membrana para uma região de baixa concentração de soluto, aplicando uma pressão que excede a pressão osmótica. É reconhecido principalmente pela sua aplicação na dessalinização da água do mar para produzir água potável, através da remoção de sais e outras substâncias indesejáveis.
Osmose direta
A osmose pode ser empregada diretamente para a separação de água de soluções contendo solutos indesejáveis. Isto envolve a utilização de uma solução de "extracção", que possui uma pressão osmótica mais elevada do que a solução de alimentação, para induzir um fluxo líquido de água através de uma membrana semipermeável. Este processo resulta na concentração da solução de alimentação e na diluição da solução de extração. A solução de extração diluída pode então ser utilizada diretamente (por exemplo, com um soluto ingerível, tal como glicose) ou direcionada para um processo de separação secundário para a remoção do soluto de extração. Dependendo das características específicas do soluto extraído e da água de alimentação, esta separação secundária pode ser potencialmente mais eficiente do que a osmose reversa independente. A osmose direta é uma área ativa de pesquisa, com aplicações que abrangem dessalinização, purificação de água, tratamento de água, processamento de alimentos e outros domínios científicos.
Desenvolvimentos Futuros em Osmose
Avanços futuros em osmose e pesquisas relacionadas apresentam um potencial significativo em diversas aplicações. Os pesquisadores estão investigando ativamente materiais avançados para aumentar a eficiência dos processos osmóticos, avançando assim nas tecnologias de dessalinização e purificação da água. Além disso, a incorporação da geração de energia osmótica, que aproveita o diferencial de pressão osmótica entre a água salina e a água doce para a produção de energia, representa uma fonte de energia sustentável e renovável com considerável promessa. Na investigação médica, a área está a explorar sistemas inovadores de administração de medicamentos baseados em princípios osmóticos, permitindo a administração precisa e controlada de medicamentos no corpo. Com a evolução contínua da tecnologia e da compreensão neste domínio, prevê-se que as aplicações da osmose se alarguem, abordando um espectro de desafios globais na sustentabilidade da água, geração de energia e cuidados de saúde.
Notas
Notas
Referências
- Simulação de osmose em Java
- Um experimento de osmose arquivado em 1º de julho de 2016 na Wayback Machine