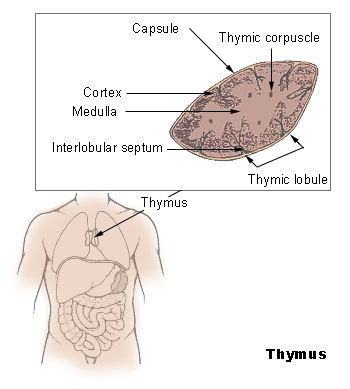
Timus (çoğul: timuslar veya timi), bağışıklık sisteminin ayrılmaz bir parçası olan özel bir birincil lenfoid organ olarak işlev görür. Bu organın içinde, adaptif bağışıklık sisteminin temel bileşenleri olan T hücreleri olgunlaşmaya uğrar ve vücudun yabancı patojenlere karşı spesifik tepkiler geliştirmesini sağlar. Anatomik olarak timus, anterior superior mediastende, göğsün üst ön bölgesinde, sternumun arkasında ve kalbin önünde yer alır. Yapısı, her biri bir kapsülle çevrelenmiş, merkezi bir medulla ve bir dış korteks içeren iki ayrı lobdan oluşur.
Timus (pl.: timuslar veya timus) bağışıklık sisteminin özelleşmiş bir birincil lenfoid organıdır. Timusun içinde T hücreleri olgunlaşır. T hücreleri, vücudun belirli yabancı istilacılara uyum sağladığı adaptif bağışıklık sistemi için kritik öneme sahiptir. Timus, göğsün üst ön kısmında, anterior superior mediastende, sternumun arkasında ve kalbin önünde bulunur. Her biri merkezi bir medulla ve bir dış korteksten oluşan ve bir kapsülle çevrelenmiş iki lobdan oluşur.
Timusun hücresel bileşimi, timosit gelişimini kolaylaştıran epitel astar hücrelerinin yanı sıra timosit olarak bilinen olgunlaşmamış T hücrelerini içerir. Başarılı T hücresi olgunlaşması iki önemli süreci içerir: vücudun MHC bağışıklık reseptörleriyle uygun etkileşim (pozitif seçim) ve kendi proteinlerine karşı reaktivitenin olmaması (negatif seçim). Timus maksimum boyutunu ve aktivitesini yenidoğan ve ergenlik öncesi dönemlerde sergiler. Daha sonra, erken ergenlikten itibaren organ, boyutunda ve fonksiyonel aktivitesinde bir azalma ile karakterize edilen, dokusunun giderek yerini yağ dokusu ile değiştiren bir evrime uğrar. Bu evrime rağmen, T hücresi gelişimi yetişkinlik boyunca devam eder.
Timik anormallikler, T hücre sayısında azalmaya ve otoimmün poliendokrin sendromu tip 1 ve miyastenia gravis dahil olmak üzere otoimmün bozuklukların ortaya çıkmasına neden olabilir. Bu tür durumlar sıklıkla timoma adı verilen timik dokudan veya lenfoma olarak bilinen T hücreleri gibi olgunlaşmamış lenfositlerden kaynaklanan malignitelerle bağlantılıdır. Timusun cerrahi olarak çıkarılmasına timektomi denir. Timusun Antik Yunanlılar tarafından anatomik bir yapı olduğu kabul edilmiş olsa da bağışıklık sistemi içindeki spesifik rolü 1960'lara kadar aydınlatılamamıştır.
Anatomik Yapı
Timus, superior anterior mediasten içinde sternumun posteriorunda yer alır ve kranyal olarak servikal bölgeye doğru uzanır. Pediatrik deneklerde timus pembemsi gri, yumuşak ve yüzeysel olarak loblu bir organ olarak ortaya çıkar. Doğumda boyutları genellikle 4-6 cm uzunluğunda, 2,5-5 cm genişliğinde ve yaklaşık 1 cm kalınlığındadır. Organ ergenliğe kadar büyür, potansiyel olarak 40-50 gr'lık bir kütleye ulaşır ve sonrasında involüsyon adı verilen bir süreçle boyutu giderek küçülür.
Timus anterior mediasten içinde yer alır. Boyundaki tiroid bezine göre aşağı pozisyondan dördüncü kostal kıkırdak seviyesine kadar uzanan, üst orta hatta birleşen iki lobdan oluşur. Bu loblar fibröz bir kapsülle çevrelenmiştir. Anatomik olarak timus, sternumun arkasında, perikardın üzerinde yer alır ve aortik ark ve ana damarlardan bir fasyal tabaka ile ayrılır. Özellikle sol brakiyosefalik ven zaman zaman timik dokuya gömülü olarak gözlemlenebilir. Servikal bölgede trakeanın anterior ve lateralinde, sternohyoid ve sternotiroid kasların derininde yer alır.
Mikroanatomi
Timus, merkezi olarak kaynaşmış iki lobdan oluşur ve organın iç kısmına vaskülarize uzantıları yansıtan bir kapsülle çevrelenir. Her lob yapısal olarak hücresel olarak yoğun bir dış korteks ve daha az yoğun bir iç medulla olarak farklılaşmıştır. Lobların daha da alt bölümlere ayrılması, kapsülden kaynaklanan ışınsal bölmelerle ayrılmış, çapı 0,5-2 mm olan daha küçük lobüller verir.
Timik korteks temel olarak timositlerden ve epitelyal hücrelerden oluşur. Olgunlaşmamış T hücreleri olan timositler, sürekli olarak medullaya uzanan bir ağ olan epitelyal retiküler hücrelerin ince dallanmış bir ağı tarafından sürdürülür. Bu retiküler ağ aynı zamanda kortikomedüller bileşke yakınındaki septa yoluyla kortekse nüfuz eden kan damarları için adventisyal bir katman oluşturur. Timus içinde tanımlanan ek hücre türleri arasında makrofajlar, dendritik hücreler ve küçük B hücreleri, nötrofiller ve eozinofil popülasyonları bulunur.
Medulla içinde epitelyal hücre ağı, kortekse kıyasla daha kaba bir yapı sergiler ve lenfoid hücre yoğunluğu nispeten daha düşüktür. Medüller epitelyal hücrelerin bir araya gelmesi, Hassall cisimcikleri (alternatif olarak timik cisimcikler olarak da adlandırılır) olarak bilinen eşmerkezli, yuva benzeri yapılar oluşturur. Bu korpüsküller, sayıları yaşla birlikte giderek artan eşmerkezli, katmanlı epitel hücrelerinden oluşur. Timus gelişimi sırasında embriyonik üçüncü faringeal keseden kaynaklanan epitel tüplerinin kalıntılarını temsil ederler.
Damar ve Sinir Desteği
Timus arteriyel beslenmesini öncelikle internal torasik ve alt tiroid arterlerinin dallarından alır; Bazen superior tiroid arterinden de katkılar gözlenir. Bu arteriyel dallar, timik kapsülün septasını geçerek, timik parankimi delmeden veya doğrudan kapsüle girmeden önce kortikomedüller bileşkeye ulaşır.
Timik damarlar tipik olarak sol brakiyosefalik vene, internal torasik vene ve alt tiroid damarlarına boşalır. Bazı durumlarda, superior vena kavaya doğrudan drenaj meydana gelir.
Timustan lenfatik drenaj, arteriyel ve venöz ağlara eşlik eden damarlarla birlikte tek yönlüdür. Bu lenfatik yollar sonuçta brakiyosefalik, trakeobronşiyal ve parasternal lenf düğümlerinde birleşir.
Timus, vagus siniri ve servikal sempatik zincirden innervasyon alır. Frenik sinirlerin dalları timik kapsüle kadar uzanırken bezin parankimine nüfuz etmez.
Anatomik Varyasyon
İki timik lob tipik olarak küçük boyut farklılıkları sergiler; sol lob sıklıkla sağın üstünde konumlanır. Ektopik timik doku, bezin üzerinde veya yakınında, bazen de tiroid içinde dağılmış olarak görülebilir. Pediatrik bireylerde timus, bazen tiroid bezinin seviyesine ulaşan değişken bir üst uzanım sergiler.
Gelişim Biyolojisi
Timositler ve timik epitel hücreleri farklı gelişimsel soylardan kaynaklanır. Timus epiteli başlangıçta üçüncü faringeal keseden iki taraflı büyümeler olarak ortaya çıkar, ara sıra dördüncü faringeal kesenin de katkılarıyla ortaya çıkar. Bu çıkıntılar posterolateral olarak çevredeki mezoderm ve nöral tepeden türetilen mezenkime doğru, ventral aortanın anterioruna doğru uzanır. Bu noktada timositler ve epitel hücreleri birleşerek bağ dokusuyla bütünleşir. Her divertikülün faringeal açıklığı daha sonra yok olur, ancak şişenin boynu geçici olarak hücresel bir kordon olarak kalır. Şişenin astar hücrelerinin daha fazla çoğalması, hücresel tomurcukların oluşumuna yol açar ve bunlar, istilacı mezoderm tarafından kapsüllenir ve izole edilir.
Epitel daha sonra hassas lobüller halinde düzenlenerek sünger benzeri bir mimariye evrilir. Eş zamanlı olarak kemik iliğinden hematopoietik öncüller gelişmekte olan timusa göç eder. Başarılı timus gelişimi, epitel ile bu hematopoietik timositler arasındaki karmaşık etkileşime bağlıdır. Ayrıca iyot hem timus gelişimi hem de fonksiyonel aktivitesi için gereklidir.
Timik İnvolüsyon
Doğum sonrası timus büyümeye devam eder ve ergenlik döneminde göreceli maksimum boyutuna ulaşır. Zirve aktivitesi fetal ve neonatal evrelerde ortaya çıkar ve ergenlik döneminde 20 ila 50 gramlık bir kütleye ulaşır. Daha sonra bez, timik evrim olarak adlandırılan bir süreç olan boyut ve fonksiyonel aktivitede ilerleyici bir azalmaya uğrar. Yaşamın ilk yılından sonra T hücrelerinin üretimi azalmaya başlar; yağ ve bağ dokuları yavaş yavaş timus hacminin bir kısmını işgal eder. Doğumda mevcut olan adipositlerin ergenlik sonrasında boyut ve sayıları önemli ölçüde artar, başlangıçta interlobüler septadan beze sızar, daha sonra korteks ve medullaya doğru uzanır. Bu süreç yaşlanmaya kadar devam eder ve genellikle 5-15 gram ağırlığa sahip olmasına rağmen timusun makroskobik veya mikroskobik olarak ayırt edilmesini zorlaştırır. Dahası, biriken kanıtlar, yaşa bağlı timik evrimin, timusa sahip omurgalı türlerinin hepsinde olmasa da çoğunda gözlemlenen korunmuş bir evrimsel süreç olduğunu göstermektedir.[40]
Bu atrofi temel olarak dolaşımdaki seks hormonlarının yüksek düzeylerine atfedilir; tersine, yetişkinlerde kimyasal veya fiziksel kısırlaştırma, timus boyutunda ve aktivitesinde artışa yol açar. Ayrıca ciddi sistemik hastalık veya insan bağışıklık yetersizliği virüsü enfeksiyonu da timik evrimi hızlandırabilir.
Fizyolojik İşlev
T-Lenfosit Olgunlaşması
Timus, hücre aracılı bağışıklıktan sorumlu bağışıklık sisteminin ayrılmaz bileşenleri olan T hücrelerinin olgunlaşmasını kolaylaştırmada çok önemli bir rol oynar. T hücreleri kemik iliğinde hematopoietik öncüller olarak ortaya çıkar ve daha sonra timosit olarak adlandırıldıkları timusa göç ederler. Timus mikroçevresinde bu hücreler, pozitif seçilimi (antijenlere karşı reaktiviteyi garanti eder) ve negatif seçimi (kendi antijenlerine karşı reaktiviteyi ortadan kaldırır) kapsayan karmaşık bir olgunlaşma sürecinden geçer. Tam olgunlaşmaya ulaştıktan sonra T hücreleri, vücutta temel immünolojik işlevleri yerine getirmek için timustan çıkar.
Her T hücresi, antijen olarak bilinen belirli bir maddeyi tanımak üzere özel olarak uyarlanmış benzersiz bir T hücresi reseptörüne (TCR) sahiptir. TCR'lerin çoğunluğu, somatik hücrelerin yüzeyinde bulunan ana doku uyumluluk kompleksi (MHC) ile etkileşime girer. MHC, spesifik bir TCR ile tam olarak eşleşen bir antijen sunduğunda, T hücresi reseptörü aktive olur. Olgun bir T hücresinin doğru bir şekilde çalışması için, MHC moleküllerine bağlanma ("pozitif seçim" olarak adlandırılır) kapasitesini göstermesi ve aynı zamanda vücudun kendi dokularından kaynaklanan kendi kendine antijenlere ("negatif seçim" olarak adlandırılır) tepki vermekten kaçınması gerekir. Pozitif seçilim süreçleri timik kortekste ortaya çıkarken, negatif seçilim timik medullada gerçekleşir. Bu gelişim aşamalarını takiben hayatta kalan T hücreleri, sfingozin-1-fosfat tarafından düzenlenen bir süreç olan timustan çıkar. Daha sonraki olgunlaşma periferik dolaşım sistemi içinde devam eder. Devam eden bu olgunlaşma, kısmen timus içinde yer alan hücreler tarafından salgılanan timulin, timopoietin ve timosinler gibi hormonlar ve sitokinlerden etkilenir.
Pozitif Seçim
T hücreleri benzersiz T hücresi reseptörleri ile karakterize edilir. Bu farklı reseptörlerin üretimi, RAG1 ve RAG2 genleri tarafından başlatılan bir gen yeniden düzenleme süreci olan V(D)J rekombinasyonunu içerir. Bu rekombinasyon hatalara karşı hassastır ve bazı timositlerin fonksiyonel T hücresi reseptörleri üretemediği, diğerlerinin ise otoreaktif T hücresi reseptörleri ürettiği durumlara yol açar. İşlevsel bir T hücresi reseptörünün başarılı bir şekilde oluşması durumunda timosit, daha sonra hücre yüzeyi proteinleri CD4 ve CD8'in eş zamanlı ekspresyonunu başlatır.
Bir T hücresinin sonraki hayatta kalması ve fenotipik gelişimi, komşu timik epitel hücreleriyle etkileşimlerine bağlıdır. Bu aşamada T hücresi reseptörü, epitel hücre yüzeyinde bulunan MHC molekülleriyle birleşir. Hiçbir reaktivite göstermeyen veya yalnızca zayıf reaktivite gösteren reseptörlere sahip T hücreleri, apoptoz yoluyla programlanmış hücre ölümüne maruz kalır. Tersine, reaktif bağlanma sergileyen T hücreleri hayatta kalacak ve çoğalacaktır. Tamamen olgun bir T hücresi CD4 veya CD8'den birini eksprese eder, ancak asla ikisini birden aynı anda eksprese etmez. Bu farklılaşma, TCR ile MHC sınıf I veya sınıf II molekülleri arasındaki bağlanma afinitesi ile belirlenir. Spesifik olarak, bir T hücresi reseptörünün öncelikle MHC sınıf I'e bağlanması tipik olarak olgun bir "sitotoksik" CD8-pozitif T hücresinin gelişmesine yol açarken, MHC sınıf II'ye güçlü bağlanma genellikle bir CD4-pozitif T hücresinin üretilmesiyle sonuçlanır.
Negatif Seçim
Vücudun endojen proteinlerine karşı reaktivite sergileyen T hücreleri, "negatif seçilim" olarak adlandırılan bir süreçle timus içinde yok edilir. Timus içindeki medüller epitel hücreleri ve dendritik hücreler, çeşitli diğer vücut dokularından kaynaklanan çok çeşitli belirgin proteinler sunar. AIRE geni bu ifadenin uyarılmasında çok önemli bir rol oynar. Kendi antijenlerine karşı güçlü reaktivite gösteren timositler apoptoz yoluyla elimine edilir. Bununla birlikte, kendi kendine antijenlere maruz kalan CD4-pozitif T hücrelerinin bir alt kümesi, T düzenleyici hücreler olarak farklılaşabilir ve varlığını sürdürebilir.
Klinik Önem
Bağışıklık Yetmezliği
Timusun T hücresi gelişiminin birincil bölgesi olarak rolü göz önüne alındığında, timik olgunlaşmayı etkileyen konjenital anomaliler bağışıklık yetmezliğini hızlandırabilir. Bu, timus bezinin genel gelişimiyle ilgili sorunlardan veya timosit olgunlaşmasındaki spesifik kusurlardan kaynaklanabilir. Bu tür bağışıklık yetersizliği şiddetli olabilir. Çoğunlukla genetik mutasyonlara bağlı erken yaşam timik aplazisi veya hipoplazisi (örneğin, DiGeorge sendromu, CHARGE sendromu veya alopesi ve timik yokluk ile karakterize edilen son derece nadir "çıplak" timus fenotipi), derin bağışıklık yetersizliğine ve viral, protozoal ve mantar enfeksiyonlarına karşı artan bir hassasiyete yol açar. FOXN1 mutasyonunun neden olduğu son derece nadir "çıplak" eksikliği sergileyen çıplak fareler, T hücresi eksikliklerini incelemek için değerli bir araştırma modeli olarak hizmet eder.
Timusla ilişkili bağışıklık yetersizliğinin en yaygın konjenital etiyolojisi, 22. kromozomdaki bir delesyondan kaynaklanan DiGeorge sendromudur. Bu genetik anomali, üçüncü ve dördüncü faringeal keselerin gelişimini bozarak timik aplazi veya hipoplaziye yol açar. bir dizi diğer ilişkili koşulun yanı sıra. Birlikte ortaya çıkan bu sorunlar arasında doğuştan kalp kusurları, ağız anormallikleri (yarık damak ve yarık dudak gibi), paratiroid bezi gelişim bozukluğu ve trakeoözofageal fistül oluşumu sayılabilir. Hastalar tipik olarak önemli ölçüde azalmış sayıda dolaşımdaki T hücresi ile başvururlar. Teşhis, floresan in situ hibridizasyon yoluyla konur ve tedavi genellikle timus transplantasyonunu içerir.
Ciddi kombine immün yetmezlik (SCID), T, B ve NK hücrelerindeki kombine eksikliklerle karakterize edilen nadir konjenital genetik bozuklukların bir koleksiyonunu kapsar. Bu sendromlar, hem B hem de T lenfositlerin öncüsü olarak görev yapan hematopoietik progenitör hücrelerin olgunlaşmasını bozan mutasyonlar tarafından hızlandırılır. SCID'nin altında, IL-2 reseptör genindeki fonksiyon kaybı mutasyonları ve adenin deaminaz enzim eksikliğine yol açan mutasyonlar da dahil olmak üzere çok sayıda genetik kusur yatıyor olabilir.
Otoimmün Hastalık
Otoimmün Poliendokrin Sendromu
Otoimmün Poliendokrin Sendromu Tip 1 (APS-1), timus içindeki genetik bir anomaliden kaynaklanan nadir, kalıtsal bir otoimmün hastalıktır. Bu durum özellikle medüller timik epitel hücrelerinde kendi kendine antijenlerin ekspresyonunu uyarmak için çok önemli olan otoimmün düzenleyici (AIRE) genindeki kusurlardan kaynaklanır. Sonuç olarak, kendi kendine antijenlerin bozulmuş ekspresyonu, endojen dokuları tolere etmek için yeterince eğitilmeyen T hücrelerinin gelişmesine, potansiyel olarak onları yabancı olarak algılamasına ve bir otoimmün yanıt başlatmasına yol açar. APS-1'den etkilenen kişiler tipik olarak çeşitli endokrin dokuları etkileyen bir otoimmün hastalık gösterir. Sıklıkla etkilenen organlar arasında tiroid bezi (hipotiroidizm), adrenal bezler (Addison hastalığı) ve vücut yüzeyleri (oral mukoza ve tırnakların kandidiyazı) yer alır ve sıklıkla TH17 hücre fonksiyon bozukluğuna atfedilir. Belirtiler genellikle çocukluk döneminde ortaya çıkar. Çok sayıda başka otoimmün durum da aynı anda ortaya çıkabilir. Terapötik müdahaleler öncelikle etkilenen belirli organların yönetimini hedefler.
Timoma ile İlişkili Çoklu Organ Otoimmünitesi
Timomaya bağlı çoklu organ otoimmünitesi (TAMA), timoma tanısı alan bireylerde bilinen bir komplikasyondur. Karakteristik olarak TAMA, timus içinde vücudun kendi dokularına karşı reaksiyon gösteren T hücrelerinin oluşumunu içerir. Bu anormal bağışıklık tepkisi, neoplastik timusun gelişmekte olan timositleri yeterince eğitememesi ve dolayısıyla kendi kendine tepki veren T hücrelerinin ortadan kaldırılmasını tehlikeye atması nedeniyle ortaya çıkar. Klinik olarak bu bozukluk, graft-versus-host hastalığında gözlenenlerle neredeyse aynı özellikleri gösterir.
Myastenia Gravis
Myastenia gravis (MG), öncelikle nöromüsküler sinyal iletimi için kritik olan asetilkolin reseptörlerini engelleyen antikorlarla karakterize edilen bir otoimmün hastalıktır. Bu durum sıklıkla timik hiperplazi veya timoma ile ilişkilidir ve bu antikorların üretimi muhtemelen anormal şekilde gelişmiş T hücrelerinden kaynaklanmaktadır. MG tipik olarak genç ila orta yaşlı yetişkinlerde ortaya çıkar ve istemli kas hareketlerinde belirgin yorgunluklara yol açar. Tanısal prosedürler, spesifik antikorların (örneğin, asetilkolin reseptörlerine veya kas spesifik kinaza karşı) tespitini ve timoma tanımlamak veya timusun değerlendirilmesi için bilgisayarlı tomografi (BT) taramalarını kapsar. Timus tutulumuyla ilgili olarak, timektomi, yani timusun cerrahi olarak çıkarılması, özellikle timoma varlığında tedavi edici bir seçenek olarak düşünülebilir. Ek tedaviler, asetilkolinin enzimatik bozunmasını engelleyerek nöromüsküler sinapslardaki etkisinin uzatılmasını içerir. Bu, piridostigmin gibi asetilkolinesteraz inhibitörlerinin uygulanmasıyla sağlanır.
Kanser
Thymomalar
Timomalar, timusun epitelyal hücrelerinden kaynaklanan neoplazmlardır. Bu tümörler ağırlıklı olarak 40 yaş üstü yetişkinleri etkiler. Tespit tipik olarak tümörlerin servikal kitle gibi semptomları tetiklemesi veya superior vena kava gibi komşu yapıların basısı; Timomalar ve timik hiperplazi ile güçlü ilişkisi göz önüne alındığında, miyastenia gravisli hastalara yönelik tarama protokolleri sırasında; veya göğüs röntgeni gibi görüntüleme yöntemlerinde tesadüfi bir keşif olarak. Hem timik hiperplazi hem de timomalar, hipogamaglobulinemi, Graves hastalığı, saf kırmızı hücre aplazisi, pernisiyöz anemi ve dermatomiyozit gibi çeşitli diğer otoimmün durumlarla bağlantılıdır ve muhtemelen T hücrelerinin çoğalmasına ilişkin negatif seçim sürecindeki eksikliklerden kaynaklanmaktadır.
Timomalar iyi huylu, iyi huylu ancak lokal olarak invazif (kapsüler transgresyondan dolayı "invaziv timoma" olarak adlandırılır) veya kötü huylu (karsinom) olarak kategorize edilir. Bu sınıflandırma öncelikle hücresel morfolojiye dayanmaktadır. Dünya Sağlık Örgütü'nün (WHO) bir sınıflandırma sistemi mevcut olmasına rağmen standart klinik uygulamada rutin olarak kullanılmamaktadır. Timusla sınırlı iyi huylu tümörler en yaygın şekli temsil eder, bunu lokal invaziv tümörler ve ardından karsinomlar takip eder. Raporlamada farklılıklar mevcut olup bazı kaynaklar malign tümör vakalarının daha yüksek olduğunu göstermektedir. İnvaziv timomalar, teknik olarak malign olarak sınıflandırılmamasına rağmen uzak anatomik bölgelere yayılma (metastaz) kapasitesine sahiptir. Timomalar epitelyal hücrelerden kaynaklansa da sıklıkla timositlerin bir bileşenini içerirler. Timomaların tedavisi tipik olarak timusun tamamının cerrahi rezeksiyonunu gerektirir. Bu tür bir müdahale aynı zamanda birlikte ortaya çıkan otoimmün rahatsızlıkların da geçici olarak iyileşmesine neden olabilir.
Lenfomalar
Timik T hücrelerinden kaynaklanan maligniteler, akut lenfoblastik löseminin (ALL) bir alt tipini oluşturur. Klinik görünümleri, teşhis metodolojileri ve tedavi stratejileri diğer ALL varyantlarıyla paraleldir. Diğer ALL tipleriyle uyumlu klinik belirtiler tipik olarak ekimoz veya kanamaya yol açan trombositopeniden kaynaklanır; enfeksiyonlara zemin hazırlayan immünsüpresyon; veya çeşitli organlara hücresel infiltrasyon, hepatomegali, splenomegali, lenfadenopati veya diğer anatomik bölgelerin tutulmasına neden olur. Hematolojik analiz, trombositopeni veya anemi gibi diğer hücre dizilerindeki eksikliklerin yanı sıra yüksek lökosit veya lenfoblast sayımlarını da gösterebilir. İmmünofenotipleme, karakteristik bir T hücresi yüzey proteini olan CD3 pozitif hücreleri tanımlar ve T hücresi olgunlaşma aşamalarının değerlendirilmesine yardımcı olur. Karyotiplemeyi de içeren sitogenetik analiz, Philadelphia translokasyonu gibi prognozu etkileyebilecek ve tedavi kararlarına rehberlik edebilecek spesifik kromozomal anormallikleri tespit edebilir. Terapötik yaklaşımlar genellikle çok ajanlı kemoterapi rejimlerini, hematopoietik kök hücre naklini ve enfeksiyonlara yönelik antibiyotik tedavisi ve kan transfüzyonları da dahil olmak üzere komplikasyonlara yönelik destekleyici bakımı içerir. Aşırı yüksek lökosit sayıları, aferez yoluyla sitoredüksiyonu gerektirebilir.
Timus içindeki minör B hücresi popülasyonundan kaynaklanan maligniteler, primer mediastinal büyük B hücreli lenfomalara (PMBL) neden olur. PMBL, Hodgkin olmayan lenfomanın nadir görülen bir alt tipini temsil eder, ancak olağandışı genetik aktivite ve zaman zaman Hodgkin lenfomalarını anımsatan mikroskobik morfoloji sergiler. Bu durum ağırlıklı olarak genç ve orta yaşlı bireyleri etkilemekte olup kadınlarda görülme sıklığı daha yüksektir. Semptomatik sunum sıklıkla superior vena kava veya üst solunum yolu dahil olmak üzere komşu mediastinal yapıların sıkışmasından kaynaklanır. Lenf nodu tutulumu sıklıkla mediastinal ve servikal bölgelerde görülür. Tanı tipik olarak immünohistokimyasal analize tabi tutulan bir biyopsiyi içerir. İmmünohistokimya, CD15'in yokluğunu gösterirken CD19, CD20 ve CD22'nin yanı sıra spesifik farklılaşma kümesi (CD) hücre yüzeyi proteinlerinin, özellikle CD30'un ekspresyonunu ortaya çıkarır. Tanıyı doğrulamak için ek belirteçler kullanılabilir. Terapötik protokoller genellikle CHOP veya EPOCH gibi standart rejimleri veya alternatif şemaları içerir. Bu rejimler tipik olarak siklofosfamid, antrasiklin, prednizon ve hematopoietik kök hücre naklinin de dahil olabileceği diğer kemoterapötik ajanlardan oluşur.
Timik Kistler
Timus bezi, genellikle çapı 4 cm'nin altında olan kistleri barındırabilir. Bu timik kistler sıklıkla tesadüfen keşfedilir ve genellikle asemptomatiktir. Anatomik dağılımları servikal bölgeyi ve mediasteni içerir. Karakteristik olarak kistler sıvıyla doludur ve çok katmanlı skuamöz veya kolumnar hücrelerden oluşan bir epitelyal astara sahiptir. Bununla birlikte, bir kistin varlığı, esas olarak komşu anatomik yapıların sıkışması yoluyla, timomalarla ilişkili komplikasyonlara benzer komplikasyonlara neden olabilir. Ayrıca, bazı kistler iç duvarlar (septa) sergileyebilir, bu da onların neoplastik lezyonlardan farklılaşmasını zorlaştırır. Tespit üzerine potansiyel tümörlere yönelik kapsamlı bir tanısal değerlendirme başlatılabilir; bu değerlendirme genellikle şüpheli bölgenin bilgisayarlı tomografisini (BT) veya manyetik rezonans görüntülemesini (MRI) içerir.
Cerrahi Eksizyon
Timektomi, timus bezinin cerrahi rezeksiyonunu ifade eder. Bu işlemin öncelikli endikasyonu yenidoğan döneminde konjenital kalp anomalilerinin düzeltilmesi için kalbe cerrahi erişimin kolaylaştırılmasıdır. Yenidoğanlarda timusun orantısız boyutu, kalbin ve onunla ilişkili büyük damarların cerrahi olarak görüntülenmesini ve manipülasyonunu engelleyebilir. Timektomi için ek endikasyonlar arasında timomaların eksizyonu ve miyastenia gravis tedavisi yer alır.
Bebeklik döneminde timik ablasyon, fonksiyonel T hücrelerinin gelişmemiş durumu nedeniyle sıklıkla ölümcül bir bağışıklık yetersizliğine yol açar. Bunun aksine, diğer lenfoid organlarda yerleşik T hücresi popülasyonları bulunan olgun bir lenfatik sisteme sahip olan daha büyük çocuklarda ve yetişkinlerde etki zayıflar. Bununla birlikte, yeni antijenlere karşı bağışıklık tepkisi oluşturma yeteneğinde bozulma, malignite vakalarında artış ve tüm nedenlere bağlı ölüm oranlarında artış olarak kendini gösterebilir.
Toplumsal ve Kültürel Yönler
Hayvanların timüs bezi, insan tüketimi için hazırlandığında bir tür tatlı ekmek olarak kabul edilir.
Tarihsel Bağlam
Timus, antik Yunanlılar tarafından, isimlendirilmesini kekik (Yunanca: θύμος) bitkisinden alarak tanınmıştır. Daha sonra bu terim, muhtemelen bezin bir kekik kümesine morfolojik benzerliğinden kaynaklanan "siğilli çıkıntı" anlamına geliyordu.
Galen, organın boyutlarının bir bireyin ömrü boyunca değişiklik gösterdiği gözlemini belgeleyen ilk kişiydi.
19. yüzyılda, status thymicolymphaticus olarak adlandırılan durum, lenfoid dokuda artış ve timus büyümesiyle karakterize ediliyordu. Daha önce ani bebek ölümü sendromuna katkıda bulunan bir faktör olduğu varsayılmış olsa da, bu terimin artık geçerliliğini yitirdiği düşünülüyor.
Timusun bağışıklık sistemi içindeki kritik rolü, 1961'de Jacques Miller tarafından açıklığa kavuşturuldu. Araştırması, bir günlük farelerden timusun cerrahi olarak çıkarılmasını içeriyordu; bu, daha sonra timik kökenleri nedeniyle T hücreleri olarak adlandırılan spesifik bir lenfosit popülasyonunda daha sonra bir eksikliğin gözlemlenmesine yol açtı. Bu keşiften önce timus, işlevsel önemi olmayan bir "evrimsel kaza" olarak büyük ölçüde göz ardı ediliyordu. 1962'de timusun olgun T hücrelerinin vücudun kendi dokularına toleransını artırmadaki işlevi ortaya çıkarıldı; çalışmalar, farelerde nakledilen timustan alınan T hücrelerinin, donör farenin dokularına karşı tolerans sergilediğini gösterdi. 1968'e gelindiğinde B hücreleri ve T hücreleri farklı lenfosit türleri olarak ayırt edildi ve T hücreleri için timik olgunlaşmanın gerekliliği ortaya çıktı. T hücresi alt tiplerinin, özellikle CD8 ve CD4'ün tanımlanması 1975 yılında gerçekleşti. Bu T hücresi alt sınıflarının olgunlaşma mekanizması (MHC reseptörlerine işlevsel olarak bağlanan hücrelerin pozitif seçimini içerir) 1990'larda anlaşıldı. Ayrıca, AIRE geninin kritik işlevi ve otoreaktif T hücrelerinin olgunlaşmasını önlemedeki negatif seçim süreci 1994 yılında anlaşıldı.
Son immünolojik gelişmeler, timusun T hücresi olgunlaşmasındaki rolünün anlaşılmasını önemli ölçüde artırdı.
Diğer Hayvanlarda Timus
Timus evrensel olarak tüm çeneli omurgalılarda bulunur, yaşa bağlı benzer atrofi sergiler ve diğer omurgalı türlerinde gözlemlenenle aynı immünolojik işlevleri yerine getirir. 2011 yılında, taşemen larvalarının solungaçlarında timoid olarak adlandırılan farklı bir timus benzeri lenfo-epitelyal oluşum tanımlandı. Hagfish ise bunun tersine, faringeal velar kaslara bağlı, çeşitli bağışıklık yanıtlarına aracılık eden bir prototimus içerir.
Timus ayrıca diğer omurgalı türlerinin çoğunda da bulunur ve insan timusuyla karşılaştırılabilecek yapısal ve işlevsel özellikler gösterir. Farelerde boyunda yer alan fazladan bir timus örneği zaman zaman belgelenmiştir. İnsanlara benzer şekilde, kobayın timüs bezi yetişkinliğe eriştiğinde doğal olarak körelir; ancak spontane bir laboratuvar mutasyonunun sonucu olan atimik tüysüz kobayda timik doku tamamen yoktur ve organ boşluğu kistik boşluklarla doludur.
Referanslar
Referanslar
Bu makale, Gray's Anatomy (1918) kitabının 20. baskısının 1273. sayfasından türetilen kamu malı metni birleştirir.
Kitaplar
- Timusta T hücresi gelişimi. Janice Yau'nun stromal sinyallemeyi ve toleransı anlatan videosu. Toronto Üniversitesi İmmünoloji ve Biyomedikal İletişim Bölümü. Yüksek Lisans Araştırma Projesi, Biyomedikal İletişimde Bilim Yüksek Lisansı. 2011.