Ósmosis (, también EE. UU.) denota la translocación neta inherente de moléculas de solvente a través de una membrana selectivamente permeable, procedente de una región de potencial hídrico elevado (caracterizada por una concentración de soluto más baja) a un área de potencial hídrico reducido (que posee una concentración de soluto más alta). Este movimiento tiene como objetivo equilibrar las concentraciones de soluto en ambos lados de la membrana. Alternativamente, puede caracterizar un proceso físico en el que cualquier disolvente atraviesa una membrana selectivamente permeable (que es permeable al disolvente pero no al soluto), separando dos soluciones de diferentes concentraciones. La ósmosis es capaz de realizar trabajo. La presión osmótica se define como la fuerza externa necesaria para impedir el movimiento neto del disolvente a través de la membrana. Esta presión es una propiedad coligativa, lo que significa que depende de la concentración molar del soluto más que de su identidad específica. El transporte osmótico se ve facilitado por el flujo viscoso del disolvente bajo un gradiente de presión.
Ósmosis (, EE.UU. también ) es el movimiento neto espontáneo de moléculas de disolvente a través de una membrana selectivamente permeable desde una región de alto potencial hídrico (región de menor concentración de soluto) a una región de bajo potencial hídrico (región de mayor concentración de soluto), en la dirección que tiende a igualar las concentraciones de soluto en ambos lados. También se puede utilizar para describir un proceso físico en el que cualquier disolvente se mueve a través de una membrana selectivamente permeable (permeable al disolvente, pero no al soluto) separando dos soluciones de diferentes concentraciones. Se puede hacer que la ósmosis funcione. La presión osmótica se define como la presión externa requerida para evitar el movimiento neto del disolvente a través de la membrana. La presión osmótica es una propiedad coligativa, lo que significa que la presión osmótica depende de la concentración molar del soluto pero no de su identidad. El transporte osmótico se produce a través de un flujo viscoso del disolvente bajo un gradiente de presión.
La ósmosis representa un mecanismo crucial dentro de los sistemas biológicos, principalmente porque las membranas biológicas exhiben semipermeabilidad. Generalmente, estas membranas son impenetrables por estructuras moleculares sustanciales y polares, como iones, proteínas y polisacáridos. Por el contrario, son permisivos con compuestos no polares o hidrofóbicos como los lípidos, junto con moléculas pequeñas como oxígeno, dióxido de carbono, nitrógeno y óxido nítrico. La permeabilidad depende de la solubilidad, la carga eléctrica, las propiedades químicas y las dimensiones del soluto. Las moléculas de agua atraviesan la membrana plasmática, la membrana tonoplasta (vacuola) o las membranas de orgánulos a través de la bicapa de fosfolípidos a través de acuaporinas, utilizando un mecanismo de flujo de poros selectivo. La ósmosis constituye el principal método por el cual el agua se transporta dentro y fuera de las células. La presión de turgencia dentro de una célula se mantiene principalmente a través de procesos osmóticos que ocurren a través de la membrana celular, entre el interior celular y su entorno comparativamente hipotónico.
Historial
Se han observado evidencias de fenómenos osmóticos desde la antigüedad, por ejemplo, en contextos relacionados con la construcción de las pirámides egipcias. Jean-Antoine Nollet proporcionó la observación documentada inicial de la ósmosis en 1748. El término "ósmosis" proviene de las palabras "endosmosis" y "exosmosis", que fueron formuladas por el médico francés René Joachim Henri Dutrochet (1776-1847) a partir de las palabras griegas ἔνδον (éndon "dentro"), ἔξω (éxō "exterior, externo"), y ὠσμός (ōsmós "empuje, impulsión"). En 1867, Moritz Traube desarrolló membranas de precipitación altamente selectivas, mejorando así la metodología y la precisión de la medición del flujo osmótico.
Descripción
La ósmosis se refiere a la translocación de un disolvente a través de una membrana semipermeable en la dirección de una mayor concentración de soluto. En contextos biológicos, el disolvente es característicamente agua, pero la ósmosis también es observable en líquidos alternativos, líquidos supercríticos e incluso gases.
Cuando una célula se sumerge en un medio acuoso, las moléculas de agua atraviesan la membrana celular desde una región caracterizada por una menor concentración de soluto hasta una con una mayor concentración de soluto. Por ejemplo, cuando una célula se sumerge en una solución salina, las moléculas de agua salen del interior celular. Por el contrario, si una célula se sumerge en agua dulce, las moléculas de agua ingresarán a la célula.
Cuando la membrana separa volúmenes idénticos de agua pura en lados opuestos, las moléculas de agua se translocan bidireccionalmente a una velocidad equivalente. En consecuencia, hay una ausencia de translocación neta de agua a través de la membrana.
La ósmosis se observa cuando se introducen rodajas de patata en una solución con una concentración elevada de sal. El agua del interior de la papa migra a la solución circundante, lo que produce una contracción celular y una reducción de la presión de turgencia. Existe una correlación directa entre la concentración de la solución salina y la magnitud de la reducción en las dimensiones y masa de la rodaja de papa.
Los jardines químicos ilustran el fenómeno osmótico dentro del dominio de la química inorgánica.
Mecanismo
El mecanismo subyacente que impulsa la ósmosis es susceptible de ser interpretado erróneamente como la dilución del agua por el soluto (lo que lleva a una disminución de la concentración de agua en el lado de la membrana con mayor concentración de soluto y, en consecuencia, provoca la difusión de agua a favor de un gradiente de concentración) o, alternativamente, como resultado de la afinidad de un soluto por el agua (reduciendo así la disponibilidad de agua libre en el lado de la membrana con mayor concentración de soluto y, por lo tanto, induciendo una translocación neta de agua hacia el soluto). Sin embargo, ambas conceptualizaciones han sido definitivamente refutadas.
El modelo de difusión de la ósmosis se considera insostenible porque la ósmosis puede facilitar el movimiento del agua a través de una membrana hacia una región de mayor concentración de agua. De manera similar, el modelo de "agua unida" es refutado por la observación de que la ósmosis opera independientemente del tamaño de la molécula del soluto (una característica de las propiedades coligativas) y su hidrofilicidad.
Describir la ósmosis con precisión requiere un marco mecánico o termodinámico, ya que fundamentalmente implica una interacción entre el soluto y el agua que contrarresta la presión que de otro modo ejercerían las moléculas de soluto libres. En particular, el calor ambiental se puede convertir en energía mecánica, como el ascenso del agua. En consecuencia, el transporte osmótico de disolvente se caracteriza como un fenómeno impulsado por la presión, en lugar de un proceso de difusión molecular aleatoria.
Numerosas explicaciones termodinámicas profundizan en el concepto de potencial químico, aclarando cómo el comportamiento del agua dentro de una solución se desvía del del agua pura. Esta divergencia surge del aumento de presión y la presencia de solutos, que colectivamente contrarrestan los cambios, manteniendo así un potencial químico constante. El teorema del virial ilustra que la atracción intermolecular entre las moléculas de agua y soluto disminuye la presión general. En consecuencia, la presión ejercida por las moléculas de agua entre sí en una solución es menor que en el agua pura, lo que permite que el agua pura impulse el movimiento dentro de la solución hasta que se logra el equilibrio de presión.
Importancia biológica
La presión osmótica sirve como mecanismo principal de soporte estructural en numerosas especies de plantas. El influjo de agua impulsado osmóticamente eleva la presión de turgencia ejercida contra la pared celular hasta que se equilibra con la presión osmótica, estableciendo así un estado estable.
Cuando una célula vegetal se sumerge en una solución hipertónica para su citoplasma, el agua sale de la célula, lo que hace que se encoja. Este proceso deja la célula flácida. En casos graves, la célula sufre plasmólisis, donde la membrana celular se desprende de la pared celular debido a una presión interna de agua insuficiente.
Por el contrario, cuando una célula vegetal se sitúa en una solución hipotónica para su citoplasma, el agua ingresa a la célula, lo que provoca su expansión y produce un estado turgente.
La ósmosis también es de vital importancia en las células humanas, donde media el transporte de agua a través de las membranas celulares. Este mecanismo es indispensable para preservar una hidratación celular adecuada, dada la sensibilidad de las células tanto a la deshidratación como a la sobrehidratación. Dentro de las células humanas, la ósmosis es fundamental para regular el equilibrio de agua y solutos, garantizando así un rendimiento celular óptimo. Las alteraciones en la presión osmótica pueden precipitar la disfunción celular, lo que subraya el papel vital de la ósmosis en el mantenimiento de la salud y la integridad estructural de las células humanas.
Bajo condiciones ambientales específicas, la ósmosis puede resultar perjudicial para los organismos. Por ejemplo, los peces de acuario de agua dulce y salada mueren rápidamente si se los introduce en agua con una salinidad inadecuada. El efecto osmótico letal de la sal de mesa sobre sanguijuelas y babosas proporciona otro ejemplo de cómo la ósmosis puede causar daño a las entidades vivientes.
Considere el escenario en el que una célula animal o vegetal se sumerge en una solución acuosa que contiene azúcar o sal.
- Si el medio circundante es hipotónico en comparación con el citoplasma de la célula, la célula absorberá agua por ósmosis.
- Si el medio es isotónico, no se producirá ningún movimiento neto de agua a través de la membrana celular.
- Por el contrario, si el medio es hipertónico en relación con el citoplasma de la célula, la célula experimentará una pérdida de agua por ósmosis.
En consecuencia, una célula colocada en una solución con una concentración de soluto más alta que su entorno interno sufrirá una crenación (arrugación), mientras que una célula situada en una solución con una concentración de soluto más baja se hinchará y potencialmente se lisará (estallará).
Factores que influyen
Presión osmótica
La ósmosis se puede contrarrestar elevando la presión en la región de mayor concentración de soluto en relación con la región de menor concentración de soluto. La fuerza por unidad de área, o presión, necesaria para inhibir el paso de agua (o cualquier otra solución altamente fluida) a través de una membrana selectivamente permeable hacia una solución más concentrada define la presión osmótica de esa solución, también conocida como turgencia. La presión osmótica se clasifica como una propiedad coligativa, lo que indica su dependencia únicamente de la concentración del soluto, en lugar de su composición o identidad química específica.
Gradiente osmótico
Un gradiente osmótico representa el diferencial de concentración entre dos soluciones separadas por una membrana semipermeable, lo que sirve para cuantificar la disparidad porcentual de un soluto disuelto específico.
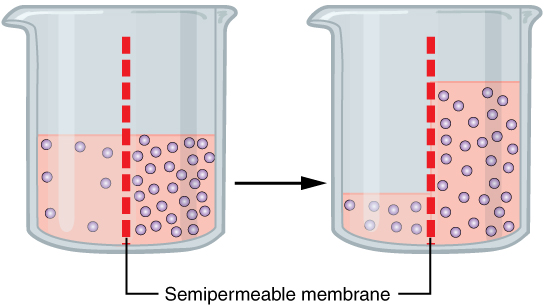
El gradiente osmótico se observa típicamente en sistemas que comprenden soluciones separadas por una membrana semipermeable, que facilita la difusión de agua hacia la solución hipertónica, caracterizada por una mayor concentración de soluto. Finalmente, la presión hidrostática ejercida por la columna de agua en el lado hipertónico se equilibra con la presión osmótica del lado hipotónico, que tiene una menor concentración de soluto, estableciendo así el equilibrio. Al alcanzar el equilibrio, el movimiento del agua persiste, pero ocurre bidireccionalmente con igual magnitud y fuerza, estabilizando así la solución.
Variaciones
Ósmosis inversa
La ósmosis inversa constituye un proceso de separación que emplea presión para impulsar un disolvente a través de una membrana semipermeable, que retiene los solutos en un lado y permite el paso del disolvente purificado al otro. Este proceso fuerza al disolvente desde una región de alta concentración de soluto a través de la membrana a una región de baja concentración de soluto aplicando una presión que excede la presión osmótica. Es principalmente reconocido por su aplicación en la desalinización de agua de mar para producir agua potable, eliminando sales y otras sustancias indeseables.
Ósmosis directa
La ósmosis se puede emplear directamente para la separación de agua de soluciones que contienen solutos indeseables. Esto implica el uso de una solución de "extracción", que posee una presión osmótica más alta que la solución de alimentación, para inducir un flujo neto de agua a través de una membrana semipermeable. Este proceso da como resultado la concentración de la solución de alimentación y la dilución de la solución de extracción. La solución de extracción diluida se puede utilizar entonces directamente (por ejemplo, con un soluto ingerible tal como glucosa) o dirigirse a un proceso de separación secundario para la eliminación del soluto de extracción. Dependiendo de las características específicas del soluto de extracción y del agua de alimentación, esta separación secundaria puede ser potencialmente más eficiente que la ósmosis inversa independiente. La ósmosis directa es un área activa de investigación, con aplicaciones que abarcan la desalinización, la purificación del agua, el tratamiento del agua, el procesamiento de alimentos y otros dominios científicos.
Futuros desarrollos en Osmosis
Los avances futuros en ósmosis y la investigación relacionada presentan un potencial significativo en diversas aplicaciones. Los investigadores están investigando activamente materiales avanzados para mejorar la eficiencia de los procesos osmóticos, avanzando así en las tecnologías de purificación y desalinización del agua. Además, la incorporación de la generación de energía osmótica, que aprovecha la diferencia de presión osmótica entre el agua salina y el agua dulce para la producción de energía, representa una fuente de energía sostenible y renovable muy prometedora. En la investigación médica, este campo está explorando sistemas innovadores de administración de fármacos basados en principios osmóticos, que permiten una administración precisa y controlada de medicamentos dentro del cuerpo. Con la continua evolución de la tecnología y los conocimientos en este ámbito, se prevé que las aplicaciones de la ósmosis se amplíen, abordando un espectro de desafíos globales en la sostenibilidad del agua, la generación de energía y la atención sanitaria.
Notas
Notas
Referencias
- Simulación de ósmosis en Java
- Un experimento de ósmosis Archivado el 1 de julio de 2016 en Wayback Machine